서론
작물은 유전적 특성과 온도와 광조건의 환경에 의해 잠재적인 수확량이 결정되지만 수분과 양분은 수확량 확보의 제한적 요소가 되며 특히 식물병, 해충 및 잡초는 수확량 감소의 주요 원인이 된다. 따라서 작물재배 시 잡초, 해충, 병원균에 대한 꾸준한 관리가 필요하다. 그 중 잡초는 영양분, 빛, 수분 등을 탈취하기 위하여 작물과 끊임없이 경합하며 잡초를 방제하지 않을 경우, 농작물의 생산량을 최대 50% 이상 감소시킬 수 있는 것으로 알려져 있다(Curran, 2016; Kaur et al., 2019). 따라서 농경지에서 잡초를 방제하는 것은 무엇보다 중요하다. 일반적으로 잡초방제방법은 물리적, 생물적, 경종적 및 화학적 방법으로 구분되며, 그 중 화학적 방제법은 유기합성 제초제을 사용하여 잡초를 방제하는 것으로, 다른 방법에 비해 효율적이고 방제 효과도 우수하여 가장 널리 사용되고 있다. 화학적 방제법에 사용되는 제초제의 최근 4년간 출하량(2019-2022)을 확인했을 때, 2019년에 4,375톤, 2022년에 5,170톤으로 제초제 사용량이 꾸준히 증가하는 모습을 보였다(KCPA, 2022). 제초제의 사용은 농업의 필수적인 부분이 되어 작물의 생산량을 증가시키고 농경지뿐만 아니라 비농경지에 발생하는 잡초를 관리하는데 중요한 역할을 하고 있지만(Cobb, 2022) 오랜 사용으로 환경오염 및 저항성 발현 등의 문제점이 지적되고 있다(Parven et al., 2024).
Gavrilescu (2005)에 따르면 농약을 처리할 때 최대 45% 수준은 목표로 하는 식물에 도달하게 되고, 나머지 55% 이상은 분해, 휘산, 흡착, 용탈(leaching) 등과 같은 방법으로 소멸하게 된다. 특히 용탈(leaching)은 제초제가 토양에서 수직 및 수평으로 이동하는 것으로 토양의 표면이나 지하수의 오염으로 이어지게 되어(Cohen et al., 1995; Whitford et al., 1999), 토양 및 수생태계에 부정적인 영향을 미칠 수 있다. 또한 제초제를 장기간 사용하면서 이에 대한 저항성 초종이 등장하고 있다(Peterson et al., 2018). 최근 보고에 의하면 2024년 기준 72개국에서 101개의 작물 경작지에서 273종(쌍자엽 156종, 단자엽 117종)의 식물이 제초제 저항성 잡초로 보고되어 있다(HRAC, 2024). 일반적으로 제초제를 식물에 처리하게 되면 침투, 이행의 과정을 거쳐 작용 부위에 축적되고 이후 목표로 하는 단백질과 결합하여 중요한 대사경로나 구조적 기능을 방해하여 세포 구성 요소에 손상을 주거나 활성 산소종 생성 등의 방법으로 세포를 손상시키고, 궁극적으로 식물을 고사시킨다. 하지만 저항성 잡초는 다양한 기작을 통해 제초 효과를 감소시키며, 크게 표적부위저항성(Target-site resistance, TSR)과 비표적부위저항성(Non-target-site resistance, NTSR)으로 구분된다. TSR은 기질-효소 간의 결합이 발생하지 않도록 표적 단백질의 구조적 돌연변이를 발생시키거나, 표적 단백질의 과다 생산을 유발하여 제초제에 대한 민감도를 현저히 감소시킨다. 한편 NTSR은 큐티클 층의 특성 및 식물의 형태 변화로 인한 제초제 침투, 이행, 축적의 감소 등의 방법으로 저항성을 나타낸다(Délye et al., 2013; Choi et al., 2024). 저항성은 방제효과가 우수하고 선택성이 확실한 제초제일수록 변화하기 쉬우며, 잡초는 종자 생산량이 많고 생육이 좋을수록 저항성이 발현되기 쉽다고 알려져있다(Park et al., 2015). 또한 저항성 잡초의 발현은 같거나 유사한 기작을 가진 제초제를 한 생물집단에 꾸준하게 사용할 경우 발생할 수 있다(Qasem, 2011).
한편 세계 생물농약 시장은 13.6%의 연평균 성장률(CAGR)로 매우 빠르게 성장하고 있다(Marrone, 2024; IR-4, 2024). 국내 생물농약 등록 현황은 2022년 12월 기준 생물살균제 70.4%, 생물살충제 22.2%, 제초제 3.7%, 기타 등이며, 전체 27품목 중 단 3품목만이 생화학농약으로 등록되어 있는 상황이다(PSIS, 2023). 생물농약은 세균, 바이러스 및 원생생물 등을 이용한 미생물농약과 자연에서 유래된 추출물 및 곤충의 페로몬 등을 이용한 생화학 농약으로 구분하며(PSIS, 2024), 생물농약의 사용은 유기합성 농약의 다양한 한계점을 해결할 수 있는 방안 중 하나이다. 그 중 생화학 농약으로 구분되는 포화지방산(saturated fatty acids)은 토양에서 생분해성(biodegradability)이 높고 독성이 낮은 친환경적인 물질이며, 특히 C6~C12 범위의 중쇄포화지방산은 잎에 직접적인 손상을 주어 세포막 파괴, 전해질 누출 등을 초래하여 식물을 고사시키는 것으로 알려져 있다(Fukuda et al., 2004). 그 중 8개의 탄소 원자를 가지는 caprylic acid (C8H1602, CAP)는 코코넛오일, 레몬그라스, 홉 등의 식물에서 확인되며 제초제뿐만 아니라 살충제, 살균제, 살비제 등으로도 사용된다(Kaczmarek et al., 2022). 탄소 원자 9개를 가지는 pelargonic acid (C9H18O2)는 pelargonium 속에서 처음 발견되었으며, 여러 식물성 오일에서 자연적으로 생산된다(Coleman and Penner, 2006, Loddo et al., 2023). 기본적으로 두 포화지방산은 burn-down 작용기작으로 잎의 왁스층을 파괴하고 식물의 세포막에 손상을 주어 짧은 시간에 급격한 건조 및 세포 누출을 유도한다(Godard et al., 2016). 특히, pelargonic acid를 처리하였을 때 15~60분 이내에 제초 활성이 발현되며 1~3시간 이내에 고사하기 시작하기 때문에 처리 후 2시간 내에 강우가 발생하더라도 제초 효과가 우수할 정도로 매우 빠른 제초 활성을 보인다고 보고되어 있다(Ciriminna et al., 2019). 이러한 특성을 가진 포화지방산은 유기합성 제초제의 다양한 한계점을 극복하여 환경친화적인 생물제초제로서 사용될 수 있을 것으로 기대된다.
Glufosinate는 방선균인 Streptomyces hygroscopicus와 S. viridochromogenes를 조사하면서 제초 특성을 가진 천연 아미노산으로 처음 발견되었다. Glufosinate는 d, l-phosphinothricin의 racemic 혼합물로 제형화되며, 그 중 암모늄염 제형이 가장 일반적으로 사용되어 glufosinate-ammonium 형태로 시중에 판매된다(Takano and Dayan`, 2020). 비선택적 접촉형 제초제이며, 무기질소 동화의 핵심적인 식물 효소인 glutamine synthase (GS)를 억제하여 NH4+ 농도가 빠르게 증가하고 glutamine이 결핍되어 궁극적으로 광호흡 및 광합성 과정이 억제되어 식물체가 고사하게 된다(Boonchaisri and Dias, 2020, Ujváry, 2010). 본 연구는 포화지방산의 제초 활성을 비교하기 위하여 국내에서 가장 일반적으로 사용하고 있는 비선택성 제초제인 glufosinate-ammonium을 대조약제로 설정하여 실험하였다.
국내 농경지에서 발생하는 잡초는 81과 619종으로 확인되며 재배지별로 발생하는 잡초를 구분하였을 때, 논에는 28과 92종, 밭에는 50과 375종, 과수원에는 63과 492종, 목초지에는 52과 275종이 발생한다고 보고되어 있다. 한편 619종 중 국화과가 96종으로 전체의 15.5%를 차지하며, 화본과가 81종으로 13.1%, 두과가 34종으로 5.5%이다(Lee et al., 2017). 그 중 Magnoliopsida (목련강) Asterales (국화목) Asteraceae (국화과) Xanthium (도꼬마리속) orientale (큰도꼬마리)의 식물분류 체계를 가지는 큰도꼬마리(정명 Xanthium orientale L., 이명 Xanthium canadense Mill.)는 북아메리카 동부 원산의 귀화식물이며 농경지뿐만아니라 길가, 버려진 공한지, 바닷가 등에서도 잘 자라는 키 0.5~2 m 정도의 한해살이풀이다(Ruggiero et al., 2015). 큰도꼬마리는 종피가 매우 두꺼워 제초제의 흡수 및 침투의 불충분으로 토양처리제 효과시험에서 방제가가 저조하여 비선택적 제초제를 적용하거나 절단하는 것이 과수원에서 큰도꼬마리를 제어하는데 더 적합하다고 보고되어있다(Kim et al., 2020). 또한 Kim (2004)의 국화과 잡초의 allelopathy 효과에 대한 연구에 따르면, 도꼬마리 추출물에 함유된 페놀 화합물(coumarin 등)에 의해 알팔파의 뿌리 생장이 크게 저해되었다. 따라서 농경지에 발생하는 도꼬마리는 뛰어난 번식력과 타감작용 등으로 인해 재배작물의 생육억제를 초래하기 때문에 효과적인 방제가 요구된다.
작물은 잡초에 비해 개체 간의 변이가 적어 제초 활성을 비교 분석하기에 적합할 것으로 판단하였다. 따라서, 큰도꼬마리 이외에 작물종의 추가 선정이 필요하다고 판단되어 잎이 넓고 줄기가 단단하여 큰도꼬마리와 형태적으로 유사한 가지를 선정하였다. 가지(Solanum melongena L.)는 Magnoliopsida (목련강) Solanales (가지목) Solanaceae (가지과) Solanum (가지속) melongena (가지)의 식물분류 체계를 갖는다(Ruggiero et al. 2015). 가지는 관속식물이며 밭에서 식용작물로 재배하는 한해살이풀이다(CBD-CHM Korea, 2023).
본 연구는 비선택성 및 접촉형 제초활성을 나타내는 포화지방산 pelargonic acid와 carpylic acid의 제초활성 특성을 비선택성 제초제 glufosinate-ammonium과 비교하여 친환경 잡초방제제의 개발 및 적용 확대 가능성을 검토하고자 수행하였다.
재료 및 방법
식물재료
광엽식물의 제초활성을 비교하기 위하여 국화과 잡초 큰도꼬마리(Xanthium orientale L.)와 가지과 작물 가지(Solanum melongena L., Asiaseed, Hybrid Eggplent, Asia Heuk Jang F1®)를 사용하였다. 시험식물의 유묘는 원예용상토(명품상토, 코코피트 47.4%, 피트모스 20%, 제오라이트 11%, 펄라이트 10%, 질석 7%, NPKO)와 밭흙(사양토)를 1:1로 혼합하여 채운 사각 플라스틱 포트(95 × 95 × 100 ㎜)에 이식하였고, 큰도꼬마리와 가지의 유묘는 본엽이 각각 4엽과 5엽으로 완전 전개될 때까지 약 7일간 순화 과정을 거친 후 사용하였다. 처리 당시 큰도꼬마리는 초장 18 ± 2.3 ㎝, 가지는 초장 20 ± 1.9 ㎝이었다. 시험물질 처리 후 조사는 균일하게 발생한 잎을 선택하였으며, 큰도꼬마리는 최하엽에서부터 두번째 대생엽 중 큰 잎을 사용하였고 가지는 최하엽에서부터 5번째 전개된 잎을 사용하였다. 생육시험은 경남 진주 소재의 경상국립대학교 내동캠퍼스 온실(20-30℃, 자연광)에서 진행되었다.
시험물질
시험물질인 포화지방산 pelargonic acid (97% tech.) 및 caprylic acid (99% tech.)는 삼전순약공업㈜(Pyeongtaek, Korea)에서 구입하여 사용하였으며 대조약제인 비선택성 제초제 glufosinate-ammonium 18% 액제는 시중에서 구입하여 사용하였다(Table 1).
처리약량은 대조약제인 glufosinate-ammonium 18% 액제의 경우 표준사용량(GLU 1,540 g ai ha-1)과 2배량(GLU 2)으로 설정하였고, pelargonic acid 97% 및 caprylic acid 99%는 각각 50, 100, 200, 400, 800 및 1,600배 희석액(PA50, PA100, PA200, PA400, PA800, PA1600 및 CAP50, CAP100, CAP200, CAP400, CAP800, CAP1600)을 조제하여 사용하였다. 포화지방산을 유화시키기 위한 계면활성제는 triton-x 100 (Samchun chemicals, Pyeongtaek, Korea)을 사용하였고, 이 때 포화지방산과 계면활성제의 비율은 9:1 (v:v) 수준으로 최적화하였다. 모든 약제는 완벽한 엽면처리 조건을 부여하기 위하여 지제부로부터 3 ㎝ 이상의 지상부 전체를 3초간 침지처리하였다.
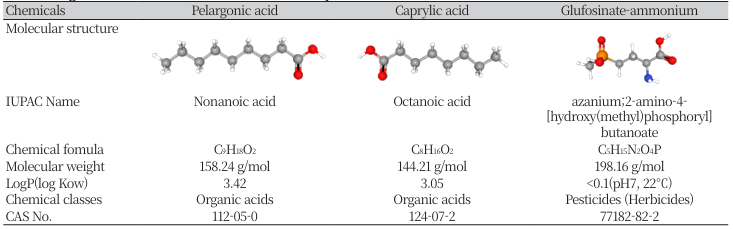
Table 1
Physicochemical properties of pelargonic acid and caprylic acid as a saturated fatty acid, non-selective herbicide glufosinate-ammonium used in this study
엽록소 함량, 생체중 및 달관평가
엽록소 함량(SPAD value)은 엽록소측정기(SPAD-502+, Konica Minolta, Osaka, Japan)로 처리 후 48, 144시간에 측정하였으며, 생체중(g)은 전자저울(HS2200S, Hansung, Seoul, Korea)을 이용하여 처리 후 144시간에 측정하였다. 엽록소 함량과 생체중은 모두 무처리 대비 변화율(%)로 구하였다. 무처리 대비 제초효과는 3, 24, 48, 72 및 144시간에 달관평가(0 ; 효과없음, 100 ; 완전고사)하였다.
엽록소 형광
엽록소 분자들에 의해 흡수된 빛 에너지는 광합성에 사용되고, 남은 에너지는 열 또는 다시 광 형태(엽록소 형광)로 소산된다. 이 3가지 과정들은 경쟁적으로 발생하고, 하나의 효율이 증가하면 나머지 두 과정의 수율을 감소시키는 형태를 나타낸다(Maxwell and Johnson. 2000). 따라서 엽록소 형광 측정을 통해 광화학 반응 및 열 소산 효율에 대한 정보를 얻을 수 있다. 본 연구에서는 비선택성 제초제 및 포화지방산 처리 후 약제에 대한 시험식물의 스트레스 정도를 확인하기 위하여 수행하였다. 엽록소 형광 측정기(PAM-2100, Walz, Germany)를 사용하여 시험물질을 처리하기 전과 처리 후 48, 72 및 144시간에 각각 측정하였다. 측정 전 약 30분간 광을 차단하여 암적응시킨 후, 큰도꼬마리와 가지의 최대양자수율(Fv/Fm, Maximum Quantum Yield of PSII))과 전자전달효율(ETR, Electron Transport Rate)을 측정하였다. 이때, 최대양자수율(Fv/Fm)은 광합성 기구의 활력도를 나타내는 지표이며 광합성능의 척도로 이용되고(Koh, 2021), 전자전달효율(ETR)은 흡수한 광 에너지에 대한 전자전달량을 의미한다(Cho et al., 2021).
전해질 누출
온실에서 생육시킨 큰도꼬마리와 가지의 잎을 직경 8 ㎜ cork borer를 이용하여 각각 20장의 엽절편을 만든 후 1% sucrose를 포함하는 1 mM 2-(N-morpholino) ethanesulfonic acid buffer (pH 6.5)가 10 ml 담겨져 있는 50 ml conical tube에 침지 처리하였고, 이는 모두 3반복으로 수행하였다. 이 때 pelargonic acid, caprylic acid는 acetone (99.5% tech.)에 녹였고, glufosinate-ammonium을 포함한 세 가지 시험물질 모두 최종 농도가 0.1%가 되도록 처리하였다. 약제를 모두 처리한 후 25℃의 생장상에서 1시간 암배양한 뒤 120 μmol m-2 s-1의 광을 조사하여 전기전도계(EC meter, CP-50N, iSTEK, Seoul, Korea)를 이용해 2시간 간격으로 10시간까지 전해물질의 누출 변화를 측정하였으며, 초기 제초 활성이 빠르게 나타나는 포화지방산의 특징을 고려하여 처리 후 1시간에도 추가적으로 측정하였다. 약제처리 농도에 따라 최초의 전도도 값이 상이하여 처리구와 무처리구에서의 차이를 약제에 의한 전도도 증가로 표시하였다(Song et al., 2004).
통계처리
모든 실험은 3반복으로 수행하였다. 통계분석은 R statistics (R-4.4.2, 2024)을 이용해 던컨다중검증 (Duncan’s multiple range test)방법으로 5% 유의수준에서 검증하였고, 그래프는 SigmaPlot (SigmaPlot 12.5, SYSTAT Software Inc, San Jose, CA, USA)을 사용하였다. 엽록소 형광은 Python 3.9의 Seaborn 0.11.1 라이브러리를 이용하여 히트맵(Heatmap) 분석하였다.
결과
엽록소 함량의 변화
큰도꼬마리의 엽록소 함량 변화는 48시간에서 포화지방산의 농도가 증가함에 따라 감소하는 경향을 보였으며, 무처리(SPAD value 40.3) 대비 최대 70%의 방제 효과를 나타내었다. 처리 후 144시간에서는 포화지방산 200배 이상의 고농도로 처리하였을 때 제초 효과가 확실하게 나타났으며, 특히 pelargonic acid는 400배 희석액 처리까지 약 70% 이상의 감소를 보였다. 대조약제인 glufosinate-ammonium의 기준량 및 배량 처리는 48시간에서 무처리 대비 각각 10.7%, 17.1% 감소하여 활성이 다소 저조하였지만, 144시간에서는 각각 48.3%, 60.5% 감소율을 보여, 시간이 경과함에 따라 제초활성이 증가하는 모습을 확인하였다(Fig. 1).
가지의 엽록소 함량의 변화도 큰도꼬마리와 유사한 경향을 나타내었다. 처리 후 48시간에서는 포화지방산 200배 희석액 처리까지 무처리 대비(SPAD value 47.4) 약 42~70%의 감소를 보였으며, 144시간에서는 포화지방산 400배 희석액 처리까지 약 64~94%의 감소를 나타내었다. 특히, pelargonic acid는 800배 희석액 처리에서도 최종적으로 61.4%의 감소율을 보였다(Fig. 2).
Fig. 1
Changes of SPAD value on cocklebur (Xanthium orientale L.) against pelargonic acid (PA, diluted from ×50 to ×1600), caprylic acid (CAP, diluted from ×50 to ×1600), and glufosinate-ammonium (GLU, recommended rate (×1), and double rate (×2)) at 48 (A) and 144 (B) hours after teatments in greenhouse condition. Bars on the graph is standard deviation. Different letters show significant differences at the level of 5% according to Duncan’s multiple range test.
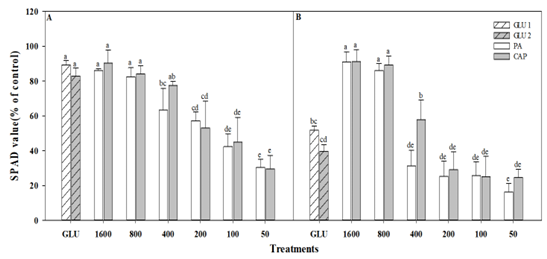
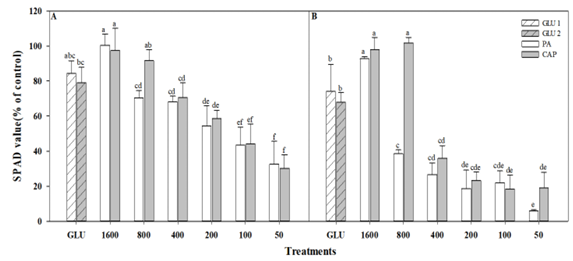
Fig. 2
Changes of SPAD value on eggplant (Solanum melongena L.) against pelargonic acid (PA, diluted from ×50 to ×1600), caprylic acid (CAP, diluted from ×50 to ×1600), and glufosinate-ammonium (GLU, recommended rate (×1), and double rate (×2)) at 48 (A) and 144 (B) hours after teatments in greenhouse condition. Bars on the graph is standard deviation. Different letters show significant differences at the level of 5% according to Duncan’s multiple range test.
생체중의 변화
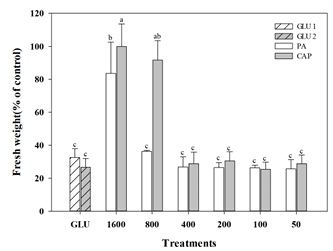
큰도꼬마리에 포화지방산을 처리한 후 144시간에 생체중을 측정하였을 때, 포화지방산 400배 희석액 처리까지 무처리 대비(15g) 약 57~82% 감소율을 보였다. 또한, glufosinate-ammonium 기준량 및 배량 처리에서도 무처리 대비 각각 69.4%, 75.8% 감소하였다(Fig. 3).
가지의 생체중은 큰도꼬마리와 유사한 결과를 보였다. 약제 처리 후 144시간에 생체중을 측정한 결과, 포화지방산은 400배 희석액 처리까지 무처리(33g) 대비 70% 이상의 감소하였고, 특히 pelargonic acid는 800배 희석액 처리에서도 63.7%의 감소율을 보였다. 이를 통해 pelargonic acid는 다른 약제에 비해 다소 낮은 농도에서도 가지 생육에 큰 영향을 미치는 것을 확인하였다(Fig. 4).
Fig. 3
Effects of inhibition of fresh weight on cocklebur (Xanthium orientale L.) against pelargonic acid (PA, diluted from ×50 to ×1600), caprylic acid (CAP, diluted from ×50 to ×1600), and glufosinate-ammonium (GLU, recommended rate (×1), and double rate (×2)) at 144 hours after teatments in greenhouse condition. Bars on the graph is standard deviation. Different letters show significant differences at the level of 5% according to Duncan’s multiple range test.
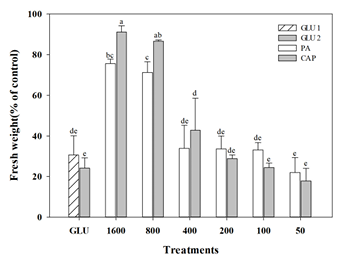
Fig. 4
Effects of inhibition of fresh weight on eggplant (Solanum melongena L.) against pelargonic acid (PA, diluted from ×50 to ×1600), caprylic acid (CAP, diluted from ×50 to ×1600), and glufosinate-ammonium (GLU, recommended rate (×1), and double rate (×2)) at 144 hours after teatments in greenhouse condition. Bars on the graph is standard deviation. Different letters show significant differences at the level of 5% according to Duncan’s multiple range test.
달관조사
큰도꼬마리에 약제처리 후 달관평가를 진행한 결과, 처리 후 3시간부터 포화지방산 일부 농도에서 수침상의 반응이 나타났다(Fig. 5). Pelargonic acid 및 caprylic acid는 200배 희석액 처리까지 90% 이상의 방제효과를 보였으며, pelargonic acid는 400배 희석액 처리에서도 70%의 제초 효과를 보였다. Fukuda 등(2004)의 다양한 탄소수를 가진 포화지방산의 제초활성을 평가한 연구 결과에 따르면, 일부 중쇄포화지방산에서 처리 후 한시간 내에 수침상의 반응과 시들음이 나타났으며 이는 본 연구 결과가 유사하였다. 대조약제는 기준량 처리 후 72시간에서 51.7%의 방제 효과를 보여 두 포화지방산 대비 다소 활성이 느린 것을 확인하였다. 이는 vista navy bean에 세 약제를(caprylic acid, pelargoinc acid, glufosinate) 처리하였을 때, caprylic acid와 pelargonic acid는 vista navy bean에 처리 후 1일부터 약 50%의 활성을 보인 반면 glufosinate는 처리 후 3일에서 약 50%의 활성을 보여 두 포화지방산이 glufosinate에 비해 제초 활성이 매우 빠르게 나타났다는 연구결과(Coleman and Penner, 2006)와 유사하였다.
가지에서도 큰도꼬마리와 유사한 경향을 나타내었다. 처리 후 3시간부터 포화지방산 일부 처리구에서 수침상의 반응이 보였으며(Fig. 6), 포화지방산 200배 희석액 처리까지 약 90%의 제초 효과를 나타내었다. 처리 후 24시간에서는 포화지방산 400배 희석액 처리까지 90% 이상의 활성을 보였고, 특히 pelargonic acid는 800배 희석액 처리에서도 81.7%로 큰도꼬마리에 비해 제초 효과가 우수하게 나타났다. Travlos 등(2020)에 따르면 서로 다른 3 종의 잡초(Avena sterilis L., Lolium rigidum Gaud, Galium aparine L.)에 pelargonic acid를 처리하였을 때, 두 잡초에 비해 큰갈퀴덩굴(Galium aparine L.)에 대한 효능이 저조하다는 결과를 나타내었다. 이를 통해 잡초 종 간에 pelargonic acid에 대한 민감도가 다르다는 사실이 확인되었으며, 큰도꼬마리와 가지에 대한 포화지방산의 제초활성 차이가 발생한 본 연구결과와 유사한 경향을 보였다.
Fig. 5
Visual effects on cocklebur (Xanthium orientale L.) against pelargonic acid (PA), caprylic acid (CAP), and glufosinate-ammonium (GLU) at 3 hours after teatments in greenhouse condition. A; pelargonic acid (diluted from ×50 to ×1600), B; caprylic acid (diluted from ×50 to ×1600), Glu; glufosinate-ammonium (recommended rate (×1), and double rate (×2)), and Control (CK).

Fig. 6
Visual effects on eggplant (Solanum melongena L.) against pelargonic acid (PA), caprylic acid (CAP), and glufosinate-ammonium (GLU) at 3 hours after teatments in greenhouse condition. A; pelargonic acid (diluted from ×50 to ×1600), B; caprylic acid (diluted from ×50 to ×1600), Glu; glufosinate-ammonium (recommended rate (×1), and double rate (×2)), and Control (CK).

엽록소 형광
큰도꼬마리는 처리 후 48시간에 최대양자수율(Fv/Fm)을 측정하였을 때, 포화지방산 50, 100, 200배 희석액 처리에서 Fv/Fm을 측정하기 어려울 만큼 생육이 크게 억제되었고, 특히 pelargonic acid는 400배 희석액 처리에서도 제초활성이 매우 높게 나타났다(Fig. 7). 한편 pelargonic acid 및 caprylic acid의 800, 1600배 희석액 처리의 Fv/Fm을 측정하였을 때에는 0.8-0.82의 수치를 나타내었다. 대부분의 식물체를 암적응시킨 후 Fv/Fm을 측정하였을 때 약 0.83의 수치를 나타내는 것으로 보아(Maxwell and Johnson, 2000) 해당 농도는 제초활성을 나타내기에 다소 낮은 농도라고 판단된다. 엽록소 형광의 매개변수 중 전자전달효율을 확인하는 ETR (Electron Transport Rate)을 측정하였을 때도 Fv/Fm의 결과와 동일하였다. 오이 자엽에 지질 생합성 및 왁스층을 표적으로 하는 제초제와 pelargonic acid를 처리하였을 때, 다른 제초제에 비해 pelargonic acid 처리에서 전자전달효율(ETR)이 매우 빠르게 감소하였다는 보고(Ciriminna et al., 2019)가 있었으며, 이는 본 연구의 결과는 유사하였다. 포화지방산과 달리, 대조약제인 glufosinate-ammnoium의 기준량 및 배량 처리구의 엽록소 형광을 측정한 결과는 Fv/Fm 및 ETR 모두 시간에 따라 완만하게 감소하는 경향을 보였다. Glufosinate-ammonium은 처리 2~5일 후 제초 활성이 나타난다는 내용(PSIS, 2024)과 일치하였으며, 포화지방산은 처리 후 15~60분 이내에 손상이 나타나기 시작해 매우 빠르게 효과가 나타난다는 연구결과(Ciriminna et al., 2019)와 유사하였다.
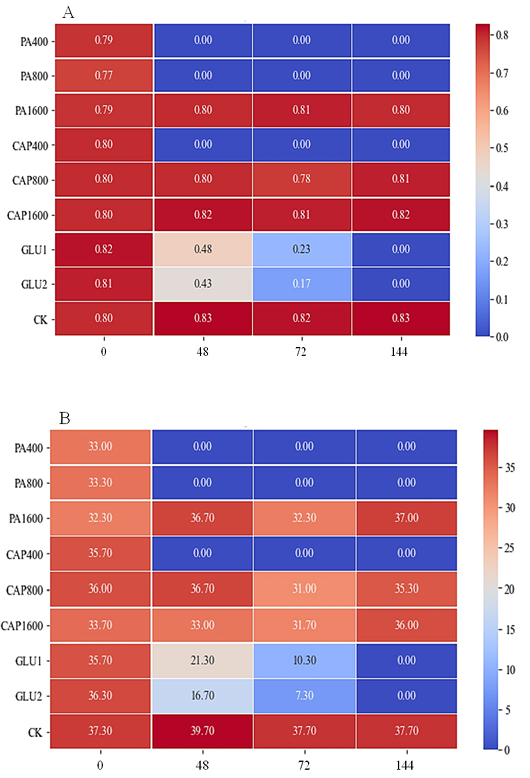
가지에서는 pelargonic acid 800배 희석액, caprylic acid 400배 희석액 처리까지 Fv/Fm 및 ETR이 급격하게 감소하면서 제초 활성이 우수하게 나타났으며(Fig. 8), 이를 통해 시험식물 간의 민감도가 다르게 나타나는 것을 재확인하였다. 대조약제인 glufosinate-ammonium의 기준량 및 배량 처리에서는 Fv/Fm 및 ETR 모두 시간이 지남에 따라 완만하게 감소하였고, 이는 큰도꼬마리와 유사하였다.
Fig. 7
Changes of chlorphyll fluorescence on cocklebur (Xanthium orientale L.) against pelargonic acid (PA, diluted from ×50 to ×1600), caprylic acid (CAP, diluted from ×50 to ×1600), and glufosinate-ammonium (GLU, recommended rate (×1), and double rate (×2)) at 0, 24, 48, and 72 hours after teatments in greenhouse condition. A; Fv/Fm(maximum quantum yield of PS II, Fv; variable fluorescence, Fm; maximum f luorescence), B; ETR (electron transport rate).
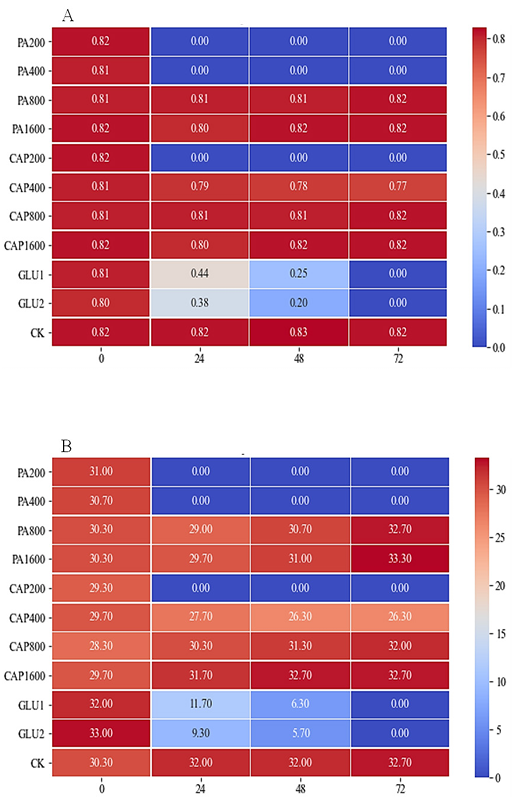
Fig. 8
Changes of chlorphyll fluorescence over time after treatments of pelargonic acid (PA), caprylic acid (CAP), and glufosinate-ammonium (GLU) treatments on eggplant (Solanum melongena L.) in greenhouse condition. A; Fv/Fm, B; ETR. Changes of chlorphyll fluorescence on eggplant (Solanum melongena L.) against pelargonic acid (PA, diluted from ×50 to ×1600), caprylic acid (CAP, diluted from ×50 to ×1600), and glufosinate-ammonium (GLU, recommended rate (×1), and double rate (×2)) at 0, 24, 48, and 72 hours after teatments in greenhouse condition. A; Fv/Fm(maximum quantum yield of PS II, Fv; variable f luorescence, Fm; maximum fluorescence), B; ETR (electron transport rate).
전해질 누출
포화지방산과 대조약제가 시험식물의 전해질 누출에 미치는 영향을 알아보기 위해 수행한 본 연구에서 두 시험물질간의 확연한 차이를 보였다. 먼저 큰도꼬마리는 처리 1시간만에 pelargonic acid 0.1% 처리에서 전도의 변화량이 50.8 μs cm-1로 다소 급격한 변화를 보였다. 처리후 10시간에서는 pelargonic acid 0.1%와 caprylic acid 0.1%에서 각각 221.3 μs cm-1, 170.7 μs cm-1의 변화량을 보여 98.8 μs cm-1의 전도의 변화량을 보인 대조약제에 비해 매우 높은 수준이었다(Fig. 9).
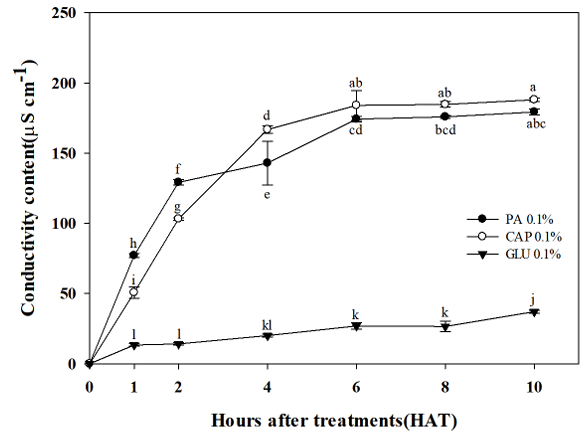
가지에서는 포화지방산 처리 후 1시간에 pelargonic acid 0.1%와 caprylic acid 0.1%에서 각각 77.1 μs cm-1, 50.7 μs cm-1로 매우 높은 수준의 변화량을 보였고, 대조약제인 glufosinate-ammonium 0.1%를 처리구에서는 두 포화지방산에 비하여 현저히 낮은 변화를 나타냈다(Fig. 10). Fukuda 등(2004)의 오이 자엽에 다양한 탄소수를 가진 포화지방산(C6-C14)을 처리하여 전해질 누출을 확인한 결과에 따르면 C9-C11에서 전해질누출율이 가장 높았으며, 특히 처리 후 1시간에서 급격하게 누출되었다. 이는 탄소수 9-11개를 가진 포화지방산이 식물 세포막 체계에 손상을 주어 매우 빠르게 생육을 억제시켰다고 보고하였으며, 이는 본 연구결과와 유사하였다.
Fig. 9
Changes of conductivity contents on cocklebur (Xanthium orientale L.) against pelargonic acid (PA, 0.1 %), caprylic acid (CAP, 0.1%), and glufosinate-ammonium (GLU, 0.1%) at 0, 1, 2, 4, 6, 8, and 10 hours after teatments in greenhouse condition. Bars on the graph is standard deviation. Different letters show significant differences at the level of 5% according to Duncan’s multiple range test.
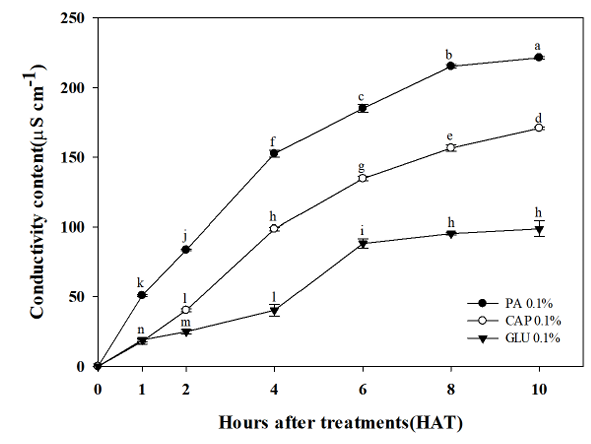
Fig. 10
Changes of conductivity contents on eggplant (Solanum melongena L.) against pelargonic acid (PA, 0.1 % ), caprylic acid (CAP, 0.1%), and glufosinate-ammonium (GLU, 0.1%) at 0, 1, 2, 4, 6, 8, and 10 hours after teatments in greenhouse condition. Bars on the graph is standard deviation. Different letters show significant differences at the level of 5% according to Duncan’s multiple range test.
고찰
제초제를 사용한 잡초 방제는 다른 방법에 비해 효율적이며 우수한 방제 효과를 보여 현재 보편적으로 사용되고 있는 방법 중 하나이다. 하지만 유기합성 제초제를 오랜 시간 사용함에 따라 환경오염 및 저항성 초종의 출현 등이 우려된다. 생물농약은 미생물, 식물추출물 및 페로몬 등을 이용하여 살충, 살균, 살초효과를 나타내는 것을 의미하며, 그 중 포화지방산은 생화학농약으로 구분되는 식물유래 천연물질이다. 포화지방산은 토양에서 생분해성이 높고 독성이 다소 낮은 특징을 가지며, 특히 탄소수에 따라 분류되는 다양한 포화지방산 중 중쇄포화지방산은 식물의 잎에 영향을 미쳐 제초활성을 나타내는 것으로 알려져 있다(Fukuda et al., 2004). 따라서, 본 연구는 포화지방산 중 pelargonic acid와 caprylic acid가 유기합성 제초제를 대신할 수 있는지 알아보기 위해 큰도꼬마리와 가지에 처리하였을 때 나타나는 제초활성을 달관평가, 전해질누출, 엽록소형광 등의 다양한 조사를 통해 확인하고자 수행하였다. 또한 제초활성을 비교 평가하기 위해 비선택성 제초제인 glufosinate-ammonium을 대조약제로 두고 실험을 진행하였다. 두 시험식물 모두 생육조사(엽록소 함량 및 생체중), 엽록소 형광 및 전해질 누출 등의 모든 조사에서 caprylic acid에 비해 pelargonic acid의 활성이 우수하였다. Fukuda 등(2004)에 따르면 지방산의 탄소 사슬이 증가할수록 소수성이 증가하며 적절한 소수성은 식물 세포막에 영향을 주는데 필수적인 요인이라고 보고하였다. 특히, pelargonic acid는 세포막을 파괴하여 식물을 고사시킬 수준의 소수성을 가지고 있어 caprylic acid에 비해 활성이 우수하게 나타난 것으로 판단된다. 또한 두 포화지방산 모두 대조약제인 glufosinate-ammonium에 비해 활성이 매우 빠르게 나타났으며, 이는 흡수, 이행의 과정을 거쳐 target-site에서 제초활성이 나타나는 glufosinate-ammonium과 달리, 접촉 후 큐티클 층과 세포막을 빠르게 파괴하여 급격한 건조를 나타내는 포화지방산의 특징에 기인한 것으로 판단된다. 활성이 매우 빠르고 우수하며 독성이 낮은 두 포화지방산의 특징을 미루어 보아, 향후 유기합성 제초제를 대신하여 다양한 잡초 방제제로서 사용될 수 있을 것으로 사료된다. 현재 pelargonic acid를 함유한 상업용 제품은 유럽을 포함한 많은 나라에서 일년생 및 다년생 잡초 방제제로 등록되어 있으며 감자의 수확 전 건조제, 이끼 및 조류에 대한 비선택적 제초제로서도 충분한 방제효과를 나타낸다고 보고되어 있다(EFSA, Alvarez et al., 2021). Caprylic acid 또한 오스트리아, 스웨덴을 포함한 일부 국가에서 제초제, 살충제, 식물생장조절제 등으로 등록되어 있다(BPDB, 2024). 국내에서도 pelargonic acid는 생물제초제로 등록되어 있지만 이원화된 법적 제도에 의해 실질적인 사용이 어려운 상황이다. 우리나라는 유기농업에 사용하기 위해서는 유기농업자재로 등록이 되어야만 사용이 가능하지만, 국내의 유기농업자재는 병해, 충해관리용자재는 있으나 잡초해관리용자재가 따로 설정되어 있지 않은 실정이다. 따라서 생물제초제의 적용 범위를 확대하고 활용성을 증가시키기 위해서는 국내의 천연식물보호제에 대한 제도적인 뒷받침이 요구된다.
요약
본 연구는 중쇄포화지방산 pelargonic acid 및 caprylic acid의 제초활성을 평가하여 유기합성 제초제를 대체할 수 있는 친환경적인 생물방제제로 사용될 수 있는지 확인하고자 수행하였다. 처리 후 48시간에서 큰도꼬마리의 포화지방산 100배 희석액 처리와 glufosinate-ammonium 기준량 처리를 비교하였을 때 무처리 대비 엽록소 함량의 감소는 각각 55-58%, 10.7%이었다. 달관평가는 각각 100%(완전고사), 18.3%로 대조약제인 glufosinate-ammonium에 비해 pelargonic acid와 caprylic acid의 제초 활성이 매우 빠르게 나타나는 것을 확인하였다. 엽록소 형광의 경우 포화지방산 처리 후 48시간보다 더 빠른 측정이 이루어져야만 평가 가능할 정도로 제초활성이 빨랐다. 가지에서도 두 약제를 비교하였을 때, 엽록소 함량의 감소는 각각 56%, 15.6%, 달관평가는 100%(완전고사), 20%이었으며, 전체적으로 큰도꼬마리와 유사한 경향이었다. 한편 포화지방산 처리구의 전해질 누출의 변화는 10시간 이내에 빠르게 발생하였다. 큰도꼬마리의 경우, pelargonic acid 0.1% 및 caprylic acid 0.1% 처리에서 각각 221.3 μs cm-1, 170.7 μs cm-1이었고, glufosinate-ammonium 0.1%는 98.8 μs cm-1의 측정치를 보였다. 가지의 경우, pelargonic acid 0.1% 및 caprylic acid 0.1% 처리에서 각각 175.9 μs cm1, 188.0 μs cm-1이었고, glufosinate-ammonium 0.1%는 37.1 μs cm-1로 현저히 낮은 측정치를 보였다. 이를 통해 pelargonic acid와 caprylic acid가 대조약제인 glufosinate-ammonium에 비해 접촉된 부위에서 매우 빠르게 제초 효과를 나타내는 것을 재차 확인하였다. 식물유래 천연물질로 토양에서 생분해성이 높고 독성이 낮은 포화지방산 중 제초 활성이 우수한 pelargonic acid 및 caprylic acid는 유기합성 제초제를 사용하기 어려운 수계 주변 잡초방제제로서 사용될 수 있으며, 수확 전 잎과 줄기를 제거해야하는 감자와 같은 작물에 수확 전 건조제로서 사용될 수 있을 것으로 사료된다. 또한 연구결과는 포화지방산을 이용한 생물방제제 개발에 대한 기초 연구자료로 사용될 것으로 판단된다.
Acknowledgements
본 연구는 제1저자(송유진)의 석사학위논문을 기반으로 작성되었음. 또한 본 연구는 2022년도 교육부의 재원으로 한국기초과학지원연구원 국가연구시설장비진흥센터에서 지원받아 수행된 연구임 (과제번호 2022R1A6C101B724).
Authors Information
Yu-Jin Song, Division of Horticultural Science, Gyeongsang National University, Master Student
In-Mo Kim, Division of Horticultural Science, Gyeongsang National University, Master Student
Myung-Soo Jin, Division of Horticultural Science, Gyeongsang National University, Master Student
Sun-Yeong Youn, Division of Horticultural Science, Gyeongsang National University, Master Student
Jeung Joo Lee, Department of Plant Medicine, Gyeongsang National University, Professor
Jeum Kyu Hong, Division of Horticultural Science, Gyeongsang National University, Professor
Sung Hwan Choi, Division of Horticultural Science, Gyeongsang National University, Professor


